办公室工作流程
1. 由我院已获得资格认定的专业作为组长单位的试验,须由申办者向机构办公室提出委托研究的申请,并出具国家食品药品监督管理总局的批件及药检部门的检测报告、临床试验方案、病例报告表、知情同意书、研究者手册以及申办方的其他相关证件等,由机构办公室对相关材料进行预审,确定符合要求后递交伦理委员会讨论。
2. 多中心的临床试验,由我院已认定的专业作为参与单位的试验,必须将相关材料(包括:药监局批件、药检报告、中心伦理委员会批件、试验方案、知情同意书、CRF表、研究者手册等)报送机构办公室预审,确定符合要求后递交本院伦理委员会审查修正至同意后,由机构办公室与申办方签署相关协议。若该试验需要申请人类遗传办,则必须在申办方递交纸质人类遗传办批件后才可签订合同并启动。
3. 机构办公室和申办者在试验开始前就试验方案、试验的监查、稽查和标准操作规程以及试验中的职责分工、不良事件发生时受试者的补偿、财务包括试验中所需支付的各种费用等相关事宜达成书面协议,并须由专业负责人签字认可。书面协议一式四份,申办方和机构各执两份,并保存至试验结束后5年。 所有的药物临床试验必须于启动会召开时正式开始。
附:办公室工作流程图
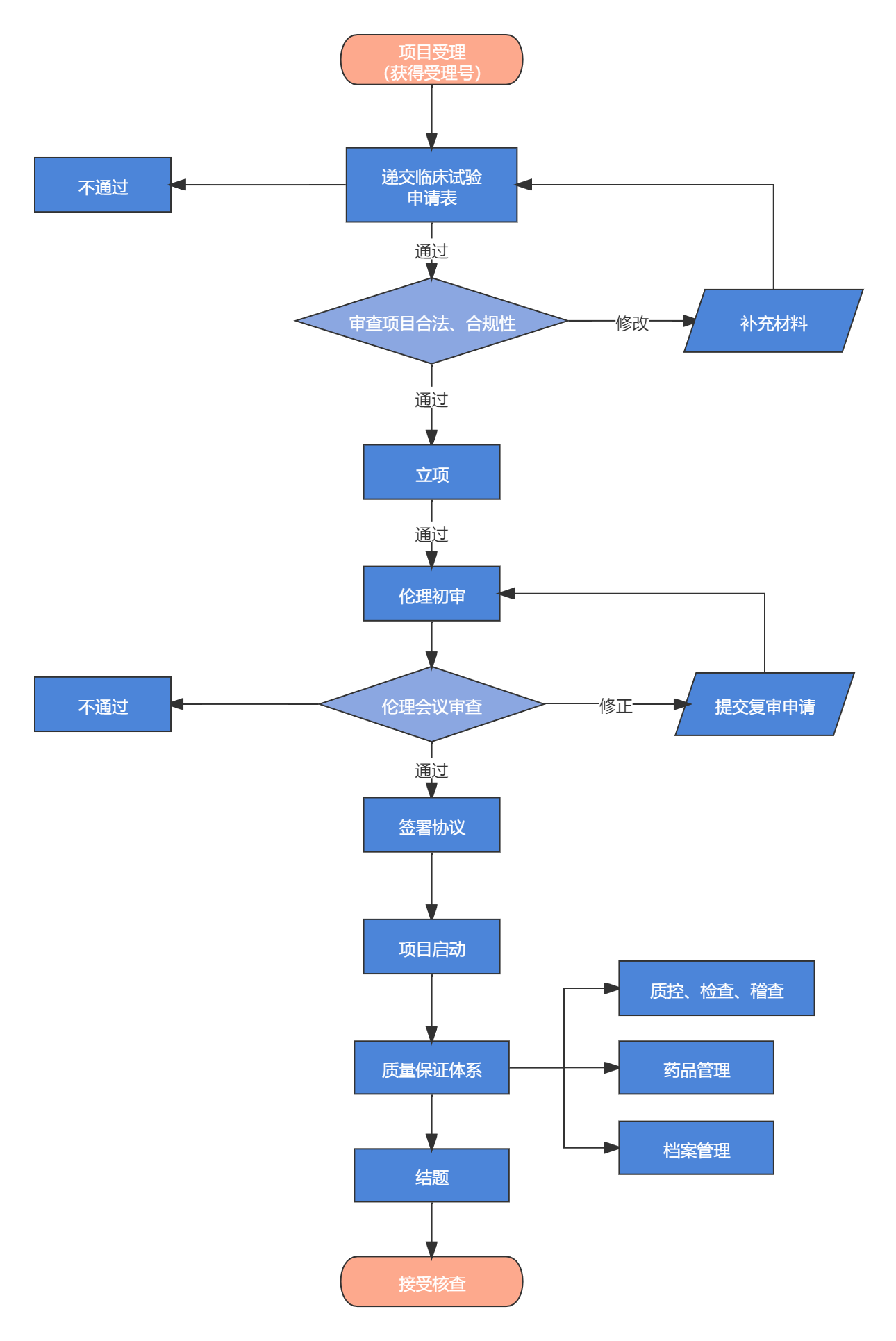
临床试验机构
About Hospital
联系电话:0535-6679498(机构办公室) 0535-6691999-82615(临床试验伦理委员会) 位于烟台毓璜顶医院行政楼21楼



